12月1日绵阳启动天气黄色预警防护措施
2023-12-02
更新时间:2023-11-29 16:38:42作者:橙橘网
导读:作为昔日一度被资本看好的“18A”医药黑马,重金押注多年的防脱发药物临床不及预期也让开拓药业多少有些“时运不济”的意思。
(文/王力 编辑/徐喆)11月29日,开拓药业-B(09939.HK)二级市场继续走低,截至发稿前,开拓药业盘中最大跌幅超7%,市值不足10亿港元。近三个交易日内公司股价累计跌幅近40%。
消息面上,开拓药业发布公告公布旗下“防脱发”治疗产品III期临床数据,结果显示,差异在统计学上与安慰剂相比并未达到显著性,而这一结果也被解读为III期临床失败。
作为开拓药业的重要管线之一,“防脱发”治疗产品曾被寄予厚望,而如今III期临床的折戟一定程度上也给公司带来一定的压力。
从现金流层面来看,前期研发投入大、时间长,如今成立十四年之久的开拓药业仍未实现商业化,而截至今年六月底,其现金及现金等价物以及定期存款合计7.02亿元,而上年度仅研发费用就支出超八亿的开拓药业如今也被市场“用脚投票”。
重金押注不及预期,值缩水不足10亿港元
11月27日,开拓药业发布公告,宣布旗下外用治疗男性雄激素性脱发(AGA)的创新药KX-826(福瑞他恩)在中国III期临床试验中读出顶线数据。
据悉,该III期临床试验是一项多中心、随机、双盲、安慰剂对照的研究,旨在评估每日使用两次外用0.5%浓度的KX-826对中国成年男性脱发患者的有效性和安全性。主要终点为治疗24周后目标区域内非毛发数(TAHC/cm2)与基线的平均变化。安全性指标包括不良事件的类型、发生率和严重程度。
分析结果显示,治疗24周后,KX-826组非撬毛数(TAHC)结果显示,KX-826与基线相比促进了毛发生长,具有统计学意义(P<0.0001)。整体而言,该试验表现出卓越的安全性,KX-826展现出良好的安全性能,并未报告任何重大不良反应。
然而,与安慰剂相比,KX-826组TAHC在各个访视点虽然均有提高,但差异在统计学上并未达到显著性。公司表示将继续对该III期临床试验的结果进行分析,并展开KX-826外用治疗脱发和痤疮的多项临床试验,不断探索KX-826上市的可能性。
这一结果直接被市场解读为III期临床失败。
作为开拓药业的重要管线产品,KX-826在之前的多个临床试验中均表现良好,这也使得外界对这款药物期待颇高。
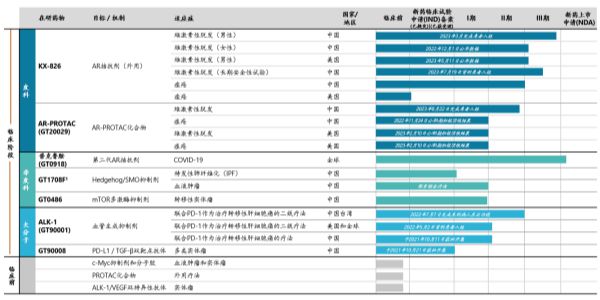
截至截至今年6月30日,开拓药业处于临床阶段的药物共有7款,除了此次的KX-826,还包括AR-PROTAC化合物(GT20029)、普克鲁胺(GT0918)、Hedgehog/SMO抑制剂(GT1708F)、mTOR激酶抑制剂(GT0486)、ALK-1抗体(GT90001)及PD-L1/TGF-β双靶点抗体(GT90008。

(图片来自开拓药业官网)
从研发进展来看,目前除了KX-826,开拓药业的GT20029同样是公司临床中用于治疗脱发的药物,同时也是全球首个进入期临床阶段的外用PROTAC化合物。
今年上半年,GT20029在中国及美国完成了脱发及痤疮适应症的期临床试验,而用于治疗脱发的中国II期临床试验已经完成了全部受试者的入组。开拓药业方面预计,明年第一季将能够公布该药物的临床实验结果。
值得一提的是,同样处于III期临床的普克鲁胺此前也曾遭遇重创。
2021年12月27日,开拓药业发布了关于其新冠药物普克鲁胺的最新进展。据治疗轻中症新冠患者的III期全球多中心临床试验中期分析数据显示,该临床试验的中期分析未达到统计学显著性。当时,市场普遍解读这一结果为开拓药业在新冠口服药物研发方面的“失败”。消息发布后,开拓药业股价一度跳水,下跌幅度超过80%。
而当前来看,作为尚未有商业化产品上市的Biotech,公司研发投入巨大也导致业绩持续亏损。
根据2023年中报,截至今年上半年,开拓药业亏损达2.12亿元,相较于2022年上半年5.18亿元的亏损,公司表示,目前的亏损主要源于研发成本和行政支出,尤其是研发成本占据了支出的主要份额。
研发投入方面,今年上半年,开拓药业的研发成本为1.65亿元,2021年和2022年,公司的研发费分别为7.68亿元和8.28亿元。
而现金流方面来看,截至2023年6月30日,开拓药业的现金及等价物以及定期存款总额为7.02亿元,另有未使用的银行融资达0.9亿元,而按照此前开拓药业的研发支出金额来看,目前公司现金储备大约只能支撑一年左右。
与此同时,管线赌局的失利,也使得公司在二级市场表现不佳。股价方面,较2021年89港元/股的高峰,彼时已跌去近97%。
国内防脱发市场有多大?
脱发可以分为瘢痕性脱发和非瘢痕性脱发,较为常见的雄激素脱发(即俗称的“雄脱”)、女性脱发、产后脱发等属于非瘢痕性脱发。
男性群体中大约70%~80%左右的脱发情况属于雄脱,女性群体的脱发原因较多,包括内分泌、甲状腺等疾病产生的脱发,铁、维生素D等微量元素的缺乏以及产后体内激素水平变化导致的脱发等。
而当前随着年轻人生活习惯和精神压力及饮食习惯的影响,脱发逐渐年轻化。脱发的提前到来,也给治疗脱发药物市场带来了一定的扩增。
当前国内市场上,已获批的药物中较为普遍的失来自辉瑞(Pfizer)公司和礼来制药的药物。
据悉,礼来和Incyte合作开发的Olumiant(巴瑞替尼)新适应症,用于治疗成人重度斑秃此前已在美国FDA宣布批准,成为FDA首个斑秃系统疗法(全身疗法)。此后今年3月27日,巴瑞替尼获得中国国家药监局(NMPA)批准成为国内首个且唯一获批用于系统性治疗重度斑秃的创新疗法。
此外,今年10月19日,中国国家药监局官网显示,批准辉瑞(Pfizer)公司申报的LITFULO™(Ritlecitinib)的上市申请,用于治疗12岁以上青少年以及成人的重度斑秃。
世界卫生组织此前公布数据显示,全球约有16亿人面临脱发问题。根据《中国人头皮健康白皮书》数据,我国脱发人口已超过2.5亿,占比高达17%,国内企业也在积极布局百亿脱发赛道。
目前,尚无国产的JAK抑制剂获批上市, 而泽璟制药(688266.SH)的杰克替尼和恒瑞医药(60276.SH)的艾玛昔替尼用于治疗斑秃适应症的临床试验进展最快,目前也进入了国内的III期阶段。
据悉,盐酸杰克替尼是泽璟制药自主研发的一种新型JAK抑制剂类药物,属于1类新药;艾玛昔替尼(SHR0302)是恒瑞医药研发的JAK1抑制剂,是1类新药,其于今年6月提交的用于治疗中重度特应性皮炎的上市许可申请已获受理。
此外科伦药业的KL130008胶囊也已进入II期临床。科笛-B(02487.HK)公布,集团治疗雄激素性脱发产品CU-40101(外用小分子甲状腺激素受体激动剂搽剂)在中国进行的I期临床试验达到主要终点。
据灼识咨询报告显示,我国脱发患者人数快速增长,预计2026年将达到3.43亿人。国内毛发医疗服务行业市场规模在2021年达到234亿元,2021年至2030年将以21.8%的复合年均增长率增长,到2030年将达到1381亿元。