传苹果将对麦克风重磅升级 iPhone 16或成公司首款AI手机?
2023-12-08
更新时间:2023-12-08 10:08:11作者:橙橘网

文/王力 编辑/徐喆
12月7日,观察者网从多地疾控中心获悉,新冠病毒XBB变异株抗原成分的疫苗已正式投放市场。专家建议符合条件的人群应及时接种该疫苗,以提高免疫防护。
十二月以来,包括丽珠集团、石药集团、神州细胞、沃森生物以及康希诺在内的五家企业的新冠疫苗被紧急纳入使用,值得注意的是,上述五家企业的五款疫苗均覆盖当下流行的XBB变异株。
当前全球范围内,新冠疫苗种类包括减毒疫苗、灭活疫苗、蛋白亚单位疫苗、病毒载体疫苗、核酸疫苗和病毒样颗粒疫苗,而随着新冠病毒不断迭代变异,哪种疫苗更为有效成了大家关注的话题。
根据中国疾病预防控制中心十一月发布的最新报告,自十月份以来,本土新冠病例的基因组有效序列表明主要为奥密克戎变异株,共涵盖73个进化分支。其中,XBB系列变异株成为主要传播株,其前三位变异株分别为XBB.1.9及其亚分支、XBB.1.22及其亚分支、XBB.1.16及其亚分支。
值得注意的是,此次沃森生物获批的新冠病毒变异株mRNA疫苗是我国首个基于完整III期安全性和有效性数据通过免疫原性桥接临床获批紧急使用的针对XBB等当前变异株的新冠mRNA疫苗,标志着中国mRNA疫苗技术自主研发能力已达到国际先进水平。
近日,在投资者互动平台,沃森生物表示公司现阶段与蓝鹊生物合作开发的产品为新冠变异株mRNA疫苗、呼吸道合胞病毒mRNA疫苗、流感病毒mRNA疫苗。此外,公司已构建起独立可控的mRNA技术平台和研发能力,并与合作方共同打造了一支国内领先的专业人才队伍。
时隔半年,国内再迎五款XBB变异株新冠疫苗
继成都威斯克重组三价XBB新冠病毒三聚体蛋白疫苗获批上市后,十二月以来国内新增五款覆盖XBB变异株的新冠疫苗获批上市。
据统计,自12月1日起至今,我国疫苗企业迎来了五款新冠疫苗的批准上市,涵盖了多个变异株的防控范围。这其中包括石药集团发布的新冠病毒二价mRNA疫苗、神州细胞研发的迭代重组新冠病毒变异株S三聚体蛋白疫苗、沃森生物的新冠病毒变异株mRNA疫苗(Omicron XBB.1.5)、康希诺推出的吸入用新冠XBB.1.5变异株疫苗(5型腺病毒载体),以及丽珠集团生产的重组新冠病毒融合蛋白二价疫苗(CHO 细胞)。
在12月1日,沃森生物(300142.SZ)和石药集团(01093.HK)先后发布公告,宣布他们所研发的新冠变异株mRNA疫苗已经获得国务院联防联控机制科研攻关组疫苗研发专班的函件,并在经过国家相关部门批准后,正式纳入紧急使用范围。
同一天晚间,神州细胞(688520.SH)也发表了公告,宣告其研发的重组新冠病毒Beta/Omicron(BA.1/BQ.1.1/XBB.1)变异株S三聚体蛋白疫苗也已被批准纳入紧急使用范围。
根据沃森生物的公告,他们获得批准上市的新冠变异株mRNA疫苗(RQ3033)是与复旦大学、蓝鹊生物合作开发的,专为应对新冠病毒Omicron XBB而设计的一款单价疫苗。与此同时,石药集团旗下的A股控股子公司石药集团新诺威制药股份有限公司(以下简称“新诺威”,300765.SZ)所获批的是新冠病毒二价mRNA疫苗(SYS6006.32),主要面向以XBB.1.5为代表的主流变异株。
而后,于12月3日晚间,丽珠集团(000513.SZ)和康希诺(688185.SH)相继宣布其研发生产的新冠疫苗获得批准,并被纳入紧急使用范围。
丽珠集团表示,由丽珠单抗研发生产的重组新型冠状病毒融合蛋白二价疫苗(CHO细胞)对EG.5.1、XBB.1.9.1、XBB.1.16、XBB.1.5等多种流行变异株均表现出广谱中和效果,显示该疫苗对当前主要流行病毒株具有良好的保护作用。康希诺在公告中提到,吸入用新冠XBB.1.5变异株疫苗将为免疫策略的更新提供助力,并为公众提供更加有效的保护。
值得注意的是,本月以来获得批准并纳入紧急使用的五款新冠疫苗都特别强调其针对本土主要流行株XBB系列变异株的保护效果。
当前,XBB系列变异株仍是我国本土疫情流行株。根据国家疾控局11月发布的数据显示,全国31个省(自治区、直辖市)及新疆生产建设兵团最新送报的本土病例新冠病毒基因组有效序列显示,均为奥密克戎变异株,涵盖73个进化分支,主要流行株为XBB系列变异株,占比前三位的分别为XBB.1.9及其亚分支、XBB.1.22及其亚分支、XBB.1.16及其亚分支。根据最新采样数据,XBB及其亚分支的占比持续高位,2023年第43周(10月23日-10月29日)已达到100.0%。
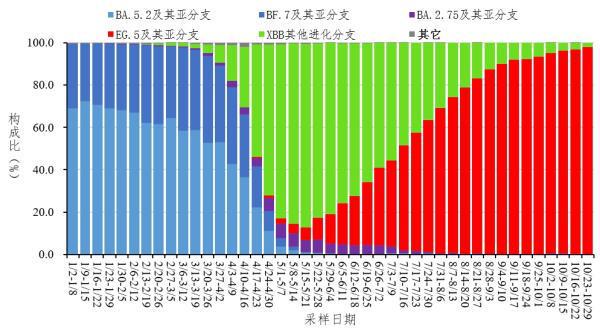
(图片来自国家疾控局)
虽XBB属于奥密克戎亚型变异毒株,其致病力和奥密克戎其他系列变异株没有明显区别,但传播力和免疫逃逸能力更高。
mRNA新冠疫苗:“广谱通用”的 “抗变异”疫苗
就在上月24日,国务院联防联控机制发布通知,要求各地加强对冬春季新冠病毒感染及其他重点传染病的防控工作。通知指出,冬春季是新冠、流感、诺如病毒胃肠炎等传染病,以及肺炎支原体感染等疾病的高发季节。
尽管目前全国新冠疫情总体平稳,但冬季我国仍面临新冠疫情反弹的风险。面对新冠病毒不断变异的情况,我国人群的血清抗体对XBB变异株的中和能力较弱,容易发生突破性感染。老年人和患有较严重基础疾病的人群等重点对象一旦感染新冠病毒XBB变异株,受害较大。
在上述五款疫苗获批上市之前,国内已经有超过10款新冠疫苗获得批准。然而,今年7月31日国务院联防联控机制综合组发布的“关于印发近期重点人群新冠病毒疫苗接种工作方案的通知”中明确提到,“在新冠病毒XBB变异株流行期间,尤其是今年秋冬季,优先推荐接种含XBB变异株抗原成分的疫苗。”
值得关注的是,新获批的五款新冠疫苗均覆盖了当前流行的XBB变异株。然而,mRNA新冠疫苗在面对病毒变异时展现出其快速适应性,能够快速设计和生产应对新变异株的疫苗。其全面性免疫作用和高度可调性使其更为有效地对抗不同变异株。
同时,mRNA新冠疫苗的生产效率高度规模化,使其能够迅速满足全球对疫苗的需求。这也意味着,mRNA新冠疫苗以其灵活性和高效性,在未来新冠变异挑战中具有明显优势。
石药集团于今年3月22日推出的新冠mRNA疫苗(SYS6006)在中国被紧急使用,并成为首个国产新冠mRNA疫苗。该疫苗覆盖了Omicron BA.5突变株的核心突变位点,对奥密克戎毒株具有较好的交叉保护效果。在5月13日,SYS6006在石家庄进行了全国首次接种,正式上市。此次新诺威子公司表示,SYS6006.32是一款针对以XBB.1.5为代表的主流变异株的mRNA疫苗。
沃森生物则表示,其研发的RQ3033疫苗是专为当前新冠病毒Omicron XBB设计的单价疫苗,符合世界卫生组织最新推荐优先使用含Omicron XBB抗原组分的单价新冠疫苗的建议。
除了在新冠预防方面的应用,mRNA技术还广泛应用于传染病和肿瘤领域。传染病领域包括流感、HIV、RSV、带状疱疹、肺结核、细菌性脑膜炎等;而肿瘤疫苗在非新冠领域的发展是mRNA技术的主要方向之一,也是各大药企寄予最高期望的领域之一。有研报预测,截至2025年,非新冠mRNA市场规模有望达到281亿美元,mRNA产业链市场前景广阔。
据不完全统计,国内已有超过10家中国企业涉足mRNA疫苗研发,其中包括石药集团、艾博生物、蓝鹊生物、康希诺、欧林生物等。